Durante décadas, los científicos han estado convencidos de que las adicciones son un problema exclusivamente cerebral. La dopamina, ese neurotransmisor que se ha vuelto casi una celebridad en redes sociales, reinaba como la reina indiscutible del sistema de recompensa. Pero resulta que el cerebro no trabaja solo. Un estudio recién publicado en Science Advances está reescribiendo lo que sabemos sobre adicción, apetito y placer, y el protagonista sorpresa es un nervio que conecta tu cerebro con tu estómago.
El nervio vago, esa autopista de información que recorre tu cuerpo desde el tronco cerebral hasta el abdomen, no solo regula tu digestión y ritmo cardíaco. También resulta ser fundamental para que experimentes el placer de comer ese pastel de chocolate o para que sientas el subidón de sustancias adictivas. Y cuando los investigadores lo cortaron en ratones de laboratorio, algo fascinante sucedió: los animales perdieron interés tanto en la comida como en las drogas.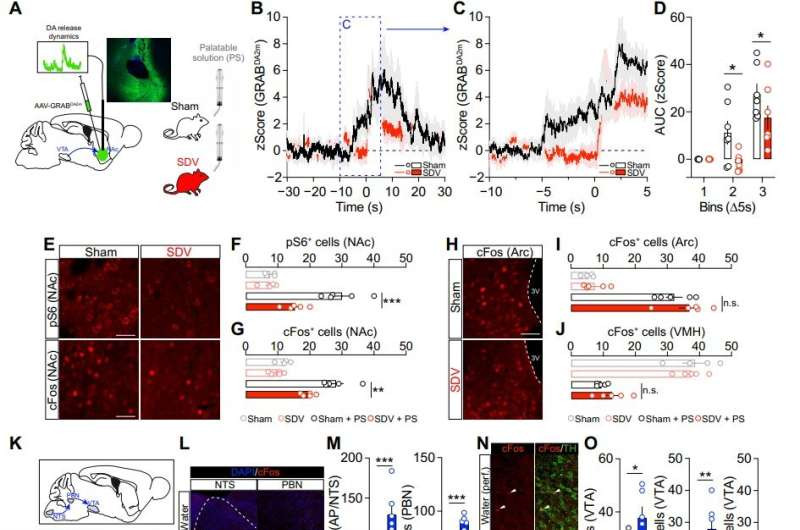
Más allá del cerebro: el eje intestino-cerebro toma el protagonismo
La investigación, liderada por un equipo multidisciplinario, utilizó una técnica llamada vagotomía subdiafragmática (SDV), que básicamente significa cortar quirúrgicamente el nervio vago. Compararon ratones con el nervio intacto (grupo control o "sham") contra ratones con el nervio cortado (grupo SDV), sometiéndolos a experimentos con alimentos altamente palatables y sustancias adictivas.
Los resultados fueron contundentes. Los ratones con el nervio vago cortado mostraron una tasa de consumo de alimentos significativamente más lenta y menor en comparación con los controles. Cuando se les ofrecía comida que normalmente encontrarían irresistible, simplemente no mostraban el mismo entusiasmo. Más impactante aún: cuando se les administraban drogas adictivas, su respuesta fue dramáticamente reducida.
Usando técnicas avanzadas como fotometría de fibra óptica, ensayos moleculares y electrofisiología, los investigadores monitorearon en tiempo real la actividad de la dopamina en los cerebros de estos ratones. Lo que descubrieron fue revelador: sin el nervio vago funcionando, la actividad de las neuronas dopaminérgicas era considerablemente menor. El sistema de recompensa, ese circuito cerebral que nos hace buscar placer y evitar el dolor, simplemente no se activaba con la misma intensidad.
El circuito mesolímbico: donde el placer se convierte en adicción
Para entender la magnitud de este descubrimiento, necesitamos hablar del circuito mesolímbico, también conocido como el "circuito de recompensa". Este sistema conecta el área tegmental ventral (VTA) con el núcleo accumbens (NAc), la amígdala y el hipocampo. Es el centro de comando que decide qué actividades vale la pena repetir para nuestra supervivencia.
Cuando comes algo delicioso, tienes sexo, o experimentas cualquier placer natural, las neuronas dopaminérgicas en el VTA se activan y liberan dopamina en el NAc. Esta explosión de dopamina no solo te hace sentir bien: le enseña a tu cerebro que esa actividad es importante y debe repetirse. Es el mismo mecanismo que utilizan las drogas adictivas, solo que estas generan oleadas de dopamina mucho más intensas que cualquier recompensa natural.
El problema con las adicciones es precisamente ese: las drogas secuestran este sistema evolutivo de supervivencia. Una oleada masiva de dopamina asociada al consumo puede reducir la liberación de dopamina incluso por debajo de los niveles basales cuando cesa el consumo, creando esa necesidad compulsiva de volver a consumir solo para sentirse "normal".
Pero aquí está el giro: lo que este nuevo estudio demuestra es que el nervio vago es esencial para que todo este sistema funcione correctamente. No es solo un mensajero pasivo que informa al cerebro sobre lo que pasa en el estómago. Es un componente activo y necesario del propio sistema de recompensa.
De la comida a la cocaína: un mecanismo compartido
Lo verdaderamente revolucionario de este hallazgo es que el nervio vago no discrimina entre tipos de recompensa. Ya sea comida altamente palatable o drogas adictivas, el mecanismo es el mismo. Esto explica por qué tantas personas en recuperación de adicciones a sustancias desarrollan problemas con la comida, o viceversa. No son "debilidades" separadas: es el mismo sistema neurobiológico en acción.
Los investigadores demostraron que la interrupción de la señalización vagal reduce tanto las respuestas de recompensa inducidas por alimentos como por drogas, atenúa la actividad de las neuronas de dopamina y altera el condicionamiento conductual a sustancias adictivas.
Esto tiene implicaciones enormes. Significa que cuando hablamos de adicción, no podemos seguir pensando solo en el cerebro. El cuerpo entero está involucrado, y específicamente, el sistema digestivo juega un papel mucho más importante de lo que nadie imaginaba.
El nervio vago: ese desconocido que hace mucho más de lo que pensábamos
El nervio vago es el décimo nervio craneal y el más largo del sistema nervioso autónomo. Su nombre significa "errante" en latín, porque literalmente vaga por todo tu torso conectando cerebro, corazón, pulmones, estómago e intestinos. Tradicionalmente se le conocía por regular funciones automáticas como la frecuencia cardíaca, la digestión y la respuesta inflamatoria.
Pero investigaciones recientes han revelado que hace mucho más. Tiene terminales aferentes (que llevan información hacia el cerebro) ubicados justo debajo del epitelio intestinal, donde pueden detectar señales producidas por la microbiota intestinal. Esa comunidad de billones de bacterias que viven en tu intestino no solo ayudan a digerir la comida: también producen neurotransmisores, metabolitos como ácidos grasos de cadena corta, y otras moléculas bioactivas que el nervio vago detecta y comunica al cerebro.
El nervio vago también regula respuestas inmunes en el intestino mediante la liberación de acetilcolina, que atenúa la activación de células inmunes. Y ahora sabemos que está directamente involucrado en el comportamiento de búsqueda de recompensas, ya sean naturales o artificiales.
Microbiota, metabolitos y adicción: una conexión que apenas comenzamos a entender
Los metabolitos microbianos, como los ácidos grasos de cadena corta (SCFA) y derivados del triptófano, regulan la síntesis y señalización de neurotransmisores, incluyendo GABA, serotonina (5-HT) y dopamina, afectando así los circuitos de recompensa y emocionales.
Esto abre una pregunta fascinante: ¿podría tu microbiota intestinal estar influyendo en tus comportamientos adictivos? La evidencia sugiere que sí. Estudios han demostrado que el consumo crónico de alcohol, estimulantes, opioides y otras drogas altera dramáticamente la composición de la microbiota intestinal, promoviendo el crecimiento de bacterias proinflamatorias y reduciendo las especies beneficiosas.
Esta disbiosis (desequilibrio microbiano) lleva a cambios en los metabolitos que producen estas bacterias. Menos ácidos grasos de cadena corta significa mayor permeabilidad intestinal (el famoso "intestino permeable"), lo que permite que endotoxinas y moléculas inflamatorias entren al torrente sanguíneo. Esto desencadena inflamación sistémica que llega hasta el cerebro, alterando aún más los circuitos de recompensa.
Es un círculo vicioso: las drogas alteran tu microbiota, la microbiota alterada produce metabolitos diferentes, esos metabolitos afectan tu cerebro a través del nervio vago, y tu cerebro modificado busca más droga. Todo conectado, todo interdependiente.
Implicaciones terapéuticas: ¿podemos hackear el nervio vago?
Si el nervio vago es esencial para el comportamiento adictivo, ¿podríamos modularlo terapéuticamente para tratar adicciones? La respuesta corta es: tal vez.
La estimulación del nervio vago (VNS, por sus siglas en inglés) ya se utiliza clínicamente para tratar epilepsia resistente a medicamentos y depresión severa. Algunos estudios preliminares han explorado su uso en adicción con resultados prometedores. Un estudio utilizó estimulación del nervio vago para extinguir comportamientos apetitivos y redujo la recaída en un modelo de rein statement de autoadministración de cocaína inducida por señales en ratas.
Pero la historia es más compleja de lo que parece. El mismo estudio encontró que los parámetros de estimulación y los paradigmas conductuales pueden producir resultados conductuales diferentes. No es tan simple como "encender" o "apagar" el nervio. Es más como afinar un instrumento musical: necesitas la frecuencia, intensidad y timing correctos.
Otra aproximación terapéutica que está ganando tracción es la modulación de la microbiota intestinal. Probióticos, prebióticos, trasplante de microbiota fecal y modificaciones dietéticas están siendo explorados como tratamientos complementarios para trastornos por uso de sustancias. La lógica es simple: si puedes restaurar una microbiota saludable, podrías normalizar las señales que viajan por el nervio vago hacia el cerebro.
Estudios preclínicos y clínicos destacan el potencial de intervenciones dirigidas a la microbiota, como probióticos, prebióticos, trasplante de microbiota fecal y modificaciones dietéticas, en restaurar la homeostasis intestinal y mejorar los resultados del tratamiento de adicciones.
Del laboratorio a la clínica: lo que aún no sabemos
Como con cualquier ciencia de frontera, hay enormes lagunas en nuestro conocimiento. Este estudio se realizó en ratones, y aunque los circuitos cerebrales de recompensa son notablemente similares entre mamíferos, los humanos somos considerablemente más complejos. Nuestras adicciones tienen componentes psicológicos, sociales y culturales que los ratones de laboratorio simplemente no experimentan.
Además, cortar el nervio vago quirúrgicamente no es exactamente una opción terapéutica viable para humanos. Los efectos secundarios serían sustanciales: problemas digestivos severos, alteración del ritmo cardíaco, dificultades respiratorias. Lo que necesitamos son métodos para modular selectivamente la señalización vagal relacionada con recompensa sin afectar sus otras funciones vitales.
También hay cuestiones éticas que considerar. Si desarrollamos tecnologías para "apagar" la respuesta de recompensa, ¿qué implicaciones tiene eso para el libre albedrío y la autonomía personal? ¿Estaríamos tratando la adicción o simplemente eliminando la capacidad de experimentar placer?
Una nueva era en la comprensión de las adicciones
Lo que este estudio deja claro es que necesitamos expandir radicalmente nuestra comprensión de las adicciones. Durante demasiado tiempo hemos pensado en ellas como un problema puramente cerebral, o peor aún, como una falla moral. La realidad es mucho más compleja y, paradójicamente, más esperanzadora.
Las adicciones son trastornos de todo el cuerpo que involucran al cerebro, el sistema digestivo, el sistema inmune, la microbiota intestinal y sus interacciones a través del nervio vago. No es solo química cerebral desbalanceada: es un ecosistema completo que ha perdido su equilibrio.
Esto abre la puerta a estrategias terapéuticas completamente nuevas. Además de los tratamientos tradicionales enfocados en el cerebro (medicamentos, psicoterapia, programas de 12 pasos), ahora podemos considerar intervenciones que apunten al eje intestino-cerebro: modificación dietética, probióticos personalizados, modulación del nervio vago, tratamiento de disbiosis intestinal.
Ninguna de estas aproximaciones será una "bala mágica". Las adicciones son demasiado complejas para eso. Pero al entender mejor los mecanismos subyacentes, podemos diseñar intervenciones más efectivas y personalizadas.
El futuro de la investigación
Los próximos pasos son claros. Necesitamos identificar exactamente qué señales está transmitiendo el nervio vago que son críticas para el comportamiento de recompensa. ¿Son metabolitos específicos? ¿Hormonas intestinales? ¿Información sobre la microbiota? Probablemente sea una combinación de todo lo anterior.
También necesitamos entender mejor la direccionalidad de estas señales. El nervio vago es bidireccional: lleva información del intestino al cerebro, pero también del cerebro al intestino. ¿Cómo se coordinan estas señales? ¿Cómo se alteran en el contexto de adicción?
Y crucialmente, necesitamos estudios en humanos. Ya hay algunos en marcha explorando la modulación del nervio vago para trastornos por uso de sustancias, pero necesitamos más: estudios más grandes, mejor diseñados, que examinen diferentes tipos de adicción y diferentes intervenciones.
Lo que está claro es que hemos entrado en una nueva era en la investigación de adicciones. Una era donde reconocemos que el cerebro no es una isla, que nuestros intestinos no solo digieren comida sino que también moldean nuestro comportamiento, y que la línea entre "mental" y "físico" es mucho más borrosa de lo que alguna vez pensamos.
Tu próximo antojo de comida chatarra o tu lucha con una adicción podrían estar siendo influenciados por billones de bacterias en tu intestino comunicándose con tu cerebro a través de un nervio que serpentea por tu torso. La ciencia a veces es más extraña que la ficción.
Y eso, paradójicamente, es una buena noticia. Porque cuanto más entendemos sobre los mecanismos reales de las adicciones, más herramientas tenemos para combatirlas.
Estudio original: "The gut-brain vagal axis is necessary for food-driven DA resealing and molecular dynamics" publicado en Science Advances (2026). DOI: 10.1126/sciadv.adz0828